Trong quá trình phản ứng PCR, thường gặp phải một số yếu tố gây nhiễu.
Do độ nhạy rất cao của PCR, sự nhiễm bẩn được coi là một trong những yếu tố quan trọng nhất ảnh hưởng đến kết quả PCR và có thể tạo ra kết quả dương tính giả.
Các nguyên nhân dẫn đến kết quả âm tính giả cũng vô cùng quan trọng. Nếu một hoặc nhiều thành phần thiết yếu của hỗn hợp PCR hoặc phản ứng khuếch đại bị ức chế hoặc bị can thiệp, xét nghiệm chẩn đoán có thể bị cản trở. Điều này có thể dẫn đến giảm hiệu quả và thậm chí là kết quả âm tính giả.
Ngoài sự ức chế, sự mất mát tính toàn vẹn của axit nucleic mục tiêu có thể xảy ra do điều kiện vận chuyển và/hoặc bảo quản trước khi chuẩn bị mẫu. Đặc biệt, nhiệt độ cao hoặc bảo quản không đúng cách có thể dẫn đến tổn thương tế bào và axit nucleic. Việc cố định tế bào và mô cũng như nhúng paraffin là những nguyên nhân nổi tiếng gây ra sự phân mảnh DNA và là một vấn đề dai dẳng (xem Hình 1 và 2). Trong những trường hợp này, ngay cả việc phân lập và tinh chế tối ưu cũng không thể giúp ích được.
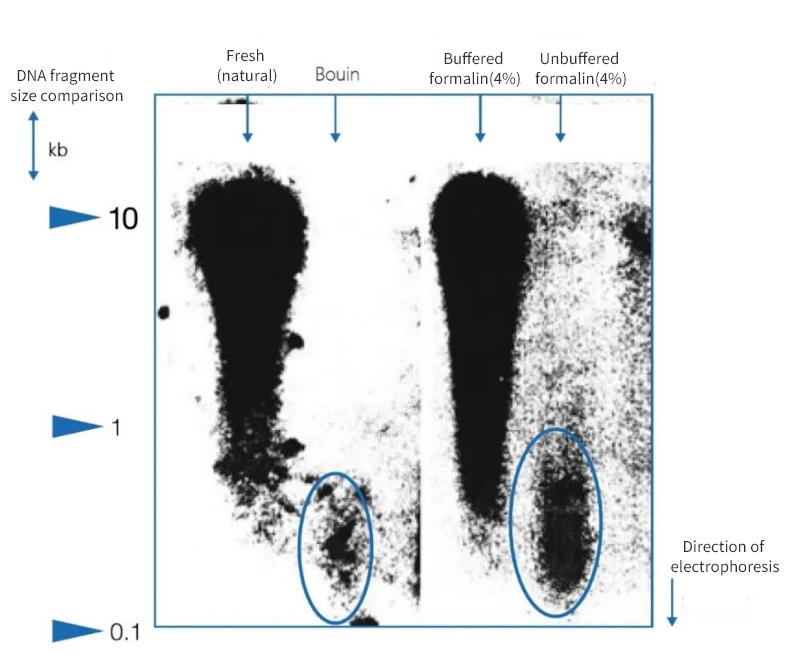
Hình 1 | Ảnh hưởng của quá trình cố định lên tính toàn vẹn của DNA
Điện di gel agarose cho thấy chất lượng DNA được phân lập từ các lát cắt mô paraffin của các mẫu khám nghiệm tử thi rất khác nhau. DNA có độ dài đoạn trung bình khác nhau xuất hiện trong các chất chiết xuất tùy thuộc vào phương pháp cố định. DNA chỉ được bảo tồn khi được cố định trong các mẫu đông lạnh nguyên trạng và trong formalin trung tính có đệm. Việc sử dụng chất cố định Bouin có tính axit mạnh hoặc formalin không có đệm, chứa axit formic dẫn đến mất mát DNA đáng kể. Phần còn lại bị phân mảnh rất nhiều.
Ở bên trái, chiều dài của các đoạn được biểu thị bằng kilobase cặp (kbp).
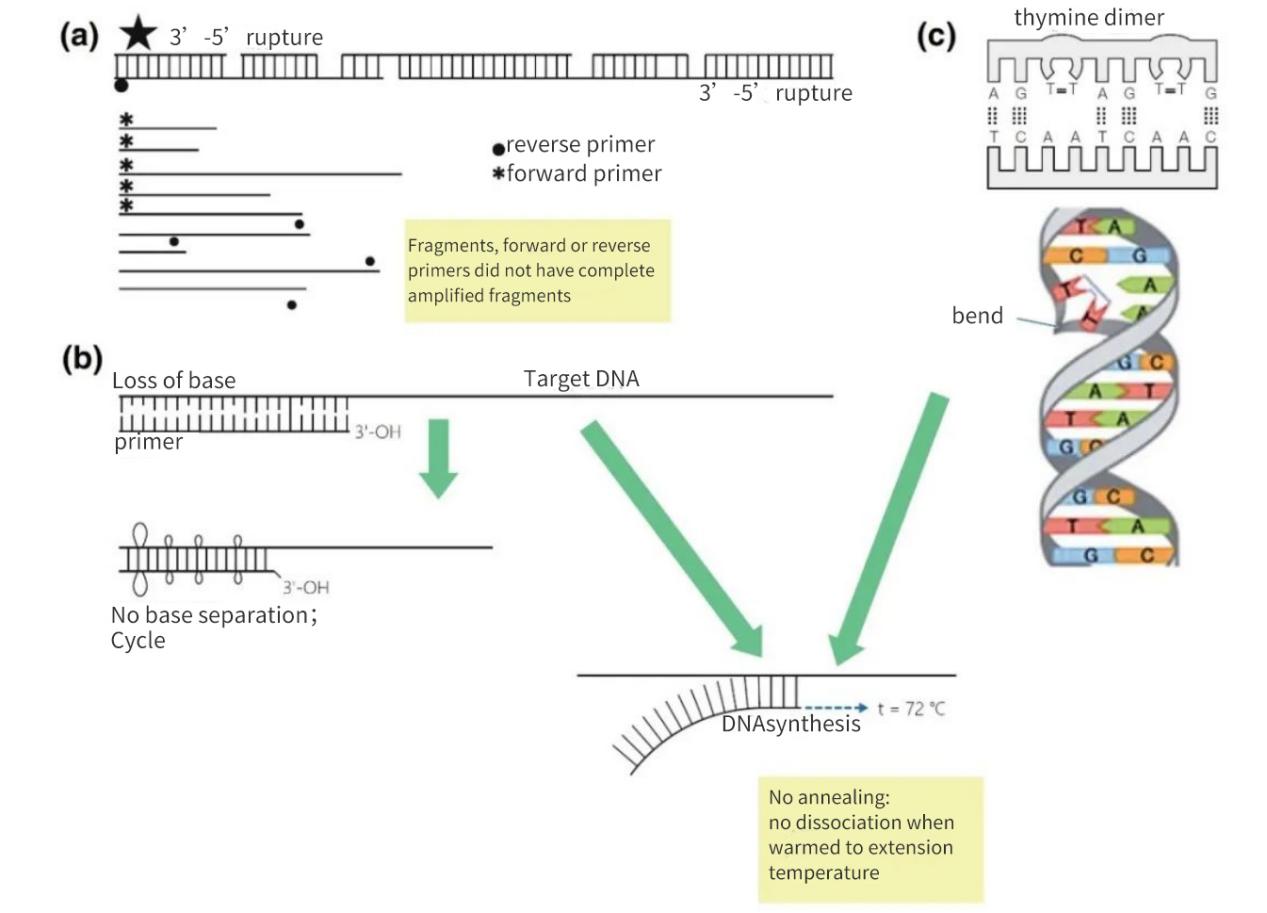
Hình 2 | Sự mất tính toàn vẹn của các mục tiêu axit nucleic
(a) Khoảng trống 3′-5′ trên cả hai mạch sẽ dẫn đến sự đứt gãy trong DNA đích. Quá trình tổng hợp DNA vẫn sẽ diễn ra trên đoạn nhỏ. Tuy nhiên, nếu vị trí gắn kết mồi bị thiếu trên đoạn DNA, chỉ có sự khuếch đại tuyến tính xảy ra. Trong trường hợp thuận lợi nhất, các đoạn có thể bão hòa lại lẫn nhau, nhưng hiệu suất sẽ thấp và dưới mức phát hiện.
(b) Sự mất các bazơ, chủ yếu do quá trình khử purin và hình thành dimer thymidine, dẫn đến giảm số lượng liên kết hydro và giảm nhiệt độ nóng chảy (Tm). Trong giai đoạn làm ấm kéo dài, các mồi sẽ tách ra khỏi DNA ma trận và sẽ không bắt cặp ngay cả trong điều kiện ít nghiêm ngặt hơn.
(c) Các bazơ thymine liền kề tạo thành một dimer TT.
Một vấn đề phổ biến khác thường xảy ra trong chẩn đoán phân tử là việc giải phóng axit nucleic mục tiêu không tối ưu so với phương pháp chiết xuất phenol-chloroform. Trong trường hợp nghiêm trọng, điều này có thể dẫn đến kết quả âm tính giả. Có thể tiết kiệm được nhiều thời gian bằng cách đun sôi tế bào hoặc tiêu hóa enzyme các mảnh vụn tế bào, nhưng phương pháp này thường dẫn đến độ nhạy PCR thấp do lượng axit nucleic giải phóng không đủ.
Ức chế hoạt động của polymerase trong quá trình khuếch đại
Nhìn chung, sự ức chế được sử dụng như một khái niệm bao hàm để mô tả tất cả các yếu tố dẫn đến kết quả PCR không tối ưu. Về mặt sinh hóa, sự ức chế chỉ giới hạn ở hoạt động của enzyme, tức là nó làm giảm hoặc ngăn chặn sự chuyển đổi chất nền thành sản phẩm thông qua tương tác với vị trí hoạt động của DNA polymerase hoặc đồng yếu tố của nó (ví dụ: Mg2+ đối với Taq DNA polymerase).
Các thành phần trong mẫu hoặc các dung dịch đệm và chất chiết xuất khác nhau có chứa thuốc thử có thể trực tiếp ức chế enzyme hoặc giữ lại các đồng yếu tố của nó (ví dụ: EDTA), do đó làm bất hoạt polymerase và dẫn đến kết quả PCR giảm hoặc âm tính giả.
Tuy nhiên, nhiều tương tác giữa các thành phần phản ứng và axit nucleic chứa mục tiêu cũng được gọi là "chất ức chế PCR". Khi tính toàn vẹn của tế bào bị phá vỡ do quá trình phân lập và axit nucleic được giải phóng, các tương tác giữa mẫu và dung dịch xung quanh cũng như pha rắn có thể xảy ra. Ví dụ, các "chất bắt giữ" có thể liên kết với DNA mạch đơn hoặc mạch đôi thông qua các tương tác không cộng hóa trị và cản trở quá trình phân lập và tinh chế bằng cách giảm số lượng mục tiêu cuối cùng đến được bình phản ứng PCR.
Nhìn chung, các chất ức chế PCR có mặt trong hầu hết các dịch cơ thể và thuốc thử được sử dụng trong các xét nghiệm chẩn đoán lâm sàng (urê trong nước tiểu, hemoglobin và heparin trong máu), thực phẩm bổ sung (các thành phần hữu cơ, glycogen, chất béo, ion Ca2+) và các thành phần trong môi trường (phenol, kim loại nặng).
| Chất ức chế | Nguồn |
| Các ion canxi | Sữa, mô xương |
| Collagen | Mô |
| Muối mật | Phân |
| Hemoglobin | Trong máu |
| Hemoglobin | Mẫu máu |
| Axit humic | Đất, cây trồng |
| Máu | Máu |
| Lactoferrin | Máu |
| (Amen châu Âu) | Da, tóc |
| Myoglobin | Mô cơ |
| Polysaccharide | Thực vật, phân |
| Protease | Sữa |
| Urê | Nước tiểu |
| Mucopolysaccharide | Sụn, màng nhầy |
| Lignin, cellulose | Thực vật |
Các chất ức chế PCR phổ biến hơn có thể được tìm thấy trong vi khuẩn và tế bào nhân chuẩn, DNA không phải mục tiêu, các đại phân tử liên kết DNA của ma trận mô và thiết bị phòng thí nghiệm như găng tay và nhựa. Tinh chế axit nucleic trong hoặc sau khi chiết xuất là phương pháp được ưu tiên để loại bỏ các chất ức chế PCR.
Hiện nay, nhiều thiết bị chiết tách tự động có thể thay thế nhiều quy trình thủ công, nhưng việc thu hồi và/hoặc tinh chế 100% các sản phẩm mục tiêu vẫn chưa bao giờ đạt được. Các chất ức chế tiềm ẩn vẫn có thể tồn tại trong axit nucleic đã được tinh chế hoặc có thể đã phát huy tác dụng. Có nhiều chiến lược khác nhau để giảm thiểu tác động của các chất ức chế. Việc lựa chọn polymerase phù hợp có thể ảnh hưởng đáng kể đến hoạt động của chất ức chế. Các phương pháp đã được chứng minh khác để giảm sự ức chế PCR là tăng nồng độ polymerase hoặc sử dụng các chất phụ gia như BSA.
Việc ức chế các phản ứng PCR có thể được chứng minh bằng cách sử dụng kiểm soát chất lượng quy trình nội bộ (IPC).
Cần hết sức cẩn thận để loại bỏ tất cả các thuốc thử và dung dịch khác trong bộ dụng cụ chiết xuất, chẳng hạn như ethanol, EDTA, CETAB, LiCl, GuSCN, SDS, isopropanol và phenol, khỏi mẫu phân lập axit nucleic bằng bước rửa kỹ. Tùy thuộc vào nồng độ của chúng, chúng có thể kích hoạt hoặc ức chế PCR.
Thời gian đăng bài: 19 tháng 5 năm 2023
 中文网站
中文网站